Yoshinori Ohsumi dostal v roku 2016 Nobelovu cenu za objav, ktorý väčšina z nás ignoruje každý deň. Nie preto, že by sme o ňom nevedeli. Preto, že náš jedálny lístok mu nedá šancu fungovať.
- 1. Paradox rastu: prečo bunka nemôže robiť dve veci naraz
- 2. Čo je autofágia — a prečo Ohsumi dostal Nobelovu cenu
- 3. Mozog, amyloid a Alzheimerova choroba: kde autofágia dostáva urgentný rozmer
- 4. Kedy sa autofágia skutočne aktivuje — bez mýtov
- 5. Čo s tým urobiť: tri prístupy podľa cieľa
- Záver: bunka, ktorá nikdy neupratuje
- Zoznam literatúry
Je pondelok ráno. Zobudíte sa, urobíte kávu, dáte si raňajky. O tri hodiny neskôr — malý snack, pretože ste čítali, že sa má jesť každé tri hodiny. Na obed polievka a chlieb. Poobede ovocie. Večer normálna večera.
Päť jedál za deň. Každé odborníkom odporúčané. Každé biologicky problematické — z jedného konkrétneho dôvodu.
Váš organizmus nikdy nedostal čas na upratovanie.
1. Paradox rastu: prečo bunka nemôže robiť dve veci naraz
Bunka má v každom momente jednu zásadnú voľbu: rásť, alebo sa opravovať.
Nie oboje naraz. Nie v rovnakej miere. Jednu z týchto aktivít vždy uprednostní — a to ktorú, závisí od toho, čo ste jedli a kedy.
Kľúčovým hráčom je enzým mTOR (mechanistic target of rapamycin) — molekulárny senzor, ktorý monitoruje dostupnosť živín v bunke. Keď je dostatok aminokyselín, glukózy a rastových faktorov, mTOR spustí anabolický program: produkcia proteínov, rast, delenie. Toto je presne to, čo chcete po tréningu alebo v mladom veku.
Ale mTOR zároveň aktívne potláča autofágiu — proces bunkového upratovania. Keď mTOR beží naplno, upratovanie sa zastaví.
A v modernom stravovaní mTOR beží takmer nepretržite. To neznamená, že autofágia nefunguje vôbec — prebieha kontinuálne na bazálnej úrovni, napríklad počas spánku. Problémom nie je jej absencia, ale chronicky znížená intenzita a skrátený čas v nízko-energetickom stave, ktorý ju optimalizuje.
2. Čo je autofágia — a prečo Ohsumi dostal Nobelovu cenu
Autofágia (z gréckeho auto — sám, phagein — jesť) je proces, pri ktorom bunka rozkladá a recykluje vlastné poškodené komponenty.
Znie to jednoducho. Mechanizmus je elegantný až zarážajúci.
Bunka identifikuje poškodený proteín alebo nefunkčnú organelu — napríklad opotrebovanú mitochondriu. Okolo tejto „odpadovej položky“ vytvorí dvojitú membránu — autofagozóm. Tento váčok sa spojí s lyzozómom, ktorého enzýmy rozložia obsah na základné stavebné jednotky: aminokyseliny, lipidy, cukry. Bunka tieto suroviny okamžite recykluje — buď na energiu, alebo na výstavbu nových štruktúr.
Je to biologická továreň na recykláciu. A funguje len, keď má priestor.
Yoshinori Ohsumi strávil desaťročia skúmaním tohto procesu na kvasinkách. V 90. rokoch identifikoval gény, ktoré autofágiu riadia — a ukázal, že sú evolučne konzervované: rovnaké gény nájdeme u kvasiniek aj u človeka. V roku 2016 za tento objav dostal Nobelovu cenu za fyziológiu a medicínu. Dôvod: autofágia nie je okrajový biologický jav. Je to fundamentálny mechanizmus, na ktorom závisí bunková integrita celého organizmu.
🔬 DEEP DIVE: Prečo sú poškodené mitochondrie časovaná bomba
Situácia zo života: Cítite sa chronicky unavení napriek dostatočnému spánku a relatívne zdravej strave. Energetické nápoje pomáhajú len krátkodobo.
Vedecké vysvetlenie: Mitochondrie — organely zodpovedné za výrobu ATP — sa dynamicky poškodzujú a obnovujú prostredníctvom procesov fúzie a delenia. Poškodené mitochondrie produkujú menej energie, ale viac voľných radikálov (reaktívnych foriem kyslíka ROS), ktoré zvyšujú oxidačný stres v bunke.
Ak sa tieto poškodené mitochondrie neodstraňujú efektívne, dochádza k ich akumulácii. Výsledkom je energetický deficit na bunkovej úrovni, zvýšený oxidačný stres a aktivácia zápalových signálnych dráh.
Proces selektívnej eliminácie poškodených mitochondrií sa nazýva mitofágia — špecifická forma autofágie.
Štúdie naznačujú, že znížená mitofágia je asociovaná s akumuláciou mitochondriálnej dysfunkcie, čo sa spája so zrýchleným biologickým starnutím svalového tkaniva a zhoršením niektorých aspektov kognitívnych funkcií.
Mitofágia sa aktivuje predovšetkým pri energetickom deficite, keď klesá aktivita mTOR a zároveň sa aktivuje energetický stresový senzor AMPK.
3. Mozog, amyloid a Alzheimerova choroba: kde autofágia dostáva urgentný rozmer
Tu prichádza časť príbehu, ktorú väčšina wellness článkov o pôste vynecháva — a ktorá mení celý pohľad na to, prečo na autofágii záleží.
Mozog spotrebúva 20 % celkovej energie organizmu. Pri takejto intenzite metabolizmu nevyhnutne vznikajú vedľajšie produkty — proteínové agregáty. Medzi najznámejšie patria amyloid beta a tau proteín — látky, ktorých nadmerná akumulácia sa spája s Alzheimerovou chorobou.
Za optimálnych fyziologických podmienok mozog tieto odpadové látky odstraňuje dvoma systémami: mikrogliami — bunkami imunitného systému mozgu — a glymfatickým systémom, ktorý je aktívny predovšetkým počas spánku.
Tretí obranný mechanizmus je autofágia neurónov.
Keď je mTOR chronicky aktívny — čo nastáva pri nepretržitej stimulácii inzulínom a aminokyselinami — autofágia v neurónoch je potlačená. Agregáty sa hromadia. Mattson a kol. (2018, Nature Reviews Neuroscience) ukázali, že prerušované fázy energetického deficitu aktivujú autofágiou závislé čistenie proteínových agregátov v mozgu a korelujú so zlepšením neuroplasticity v zvieracích modeloch. Dôležitá výhrada: väčšina týchto dôkazov pochádza zo zvieracích modelov. Priamy klinický dôkaz, že pôst zabraňuje alebo spomaľuje Alzheimerovu chorobu u ľudí, zatiaľ chýba. Mechanizmus je biologicky hodnoverný — klinické uzavretie ešte nie.
Toto nie je argument pre drastický pôst. Je to argument pre to, že mozog potrebuje čas na upratovanie — a nepretržité jedenie mu tento čas nedáva.
🔬 DEEP DIVE: Imunitný systém a autofágia — spojenie, o ktorom sa takmer nepíše
Situácia zo života: Po každej chrípke sa uzdravujete pomalšie ako pred desiatimi rokmi. Imunita „nestíha“.
Vedecké vysvetlenie: V gerontológii sa skúma jav nazývaný imunosenescencia — postupné znižovanie kvality imunitnej odpovede so starnutím. Jedným z mechanizmov je akumulácia starých, nefunkčných imunitných buniek, ktoré zaberajú miesto, ale reagujú pomaly. Autofágia umožňuje selektívnu elimináciu týchto afunkčných buniek. Po fáze autofagickej „reorganizácie“ kmeňové bunky kostnej drene dostávajú signál na proliferáciu nových imunitných buniek. Výskumy (Levine & Kroemer, 2019, Cell) naznačujú, že cykly obmedzenia živín a ich obnovy môžu prispievať k „rejuvenizácii“ imunitnej bunkovej populácie. Nejde o oslabenie imunity počas pôstu — je to dočasná reorganizácia smerom k mladšiemu bunkovému profilu.
4. Kedy sa autofágia skutočne aktivuje — bez mýtov
Tu je kde väčšina populárnych článkov zlyháva: autofágia nie je binárny prepínač, ktorý sa zapne presne po 16 hodinách.
Je to kontinuálne regulovaný proces závislý od kombinácie faktorov:
Pokles inzulínu — primárny signál. Inzulín aktivuje mTOR. Keď inzulín klesá, mTOR sa inhibuje a autofágia má priestor.
Vyčerpanie glykogénu — zásoby cukru v pečeni a svaloch. Kým sú zásoby plné, bunka nemá dôvod na internú recykláciu. Vyčerpanie trvá rôzne dlho závisí od posledného jedla, pohybovej aktivity a individuálneho metabolizmu.
Aktivácia AMPK — energetický senzor bunky. Keď bunka zaznamená nízku hladinu ATP, AMPK sa aktivuje a inhibuje mTOR — čím otvára cestu autofágii.
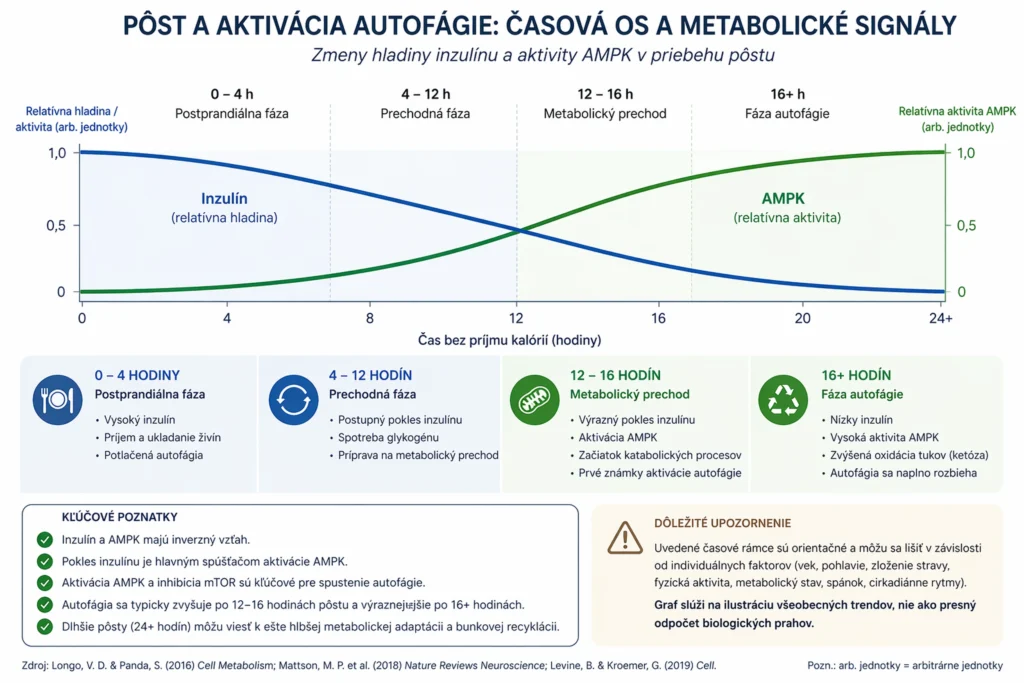
Orientačné fázy (s dôležitou výhradou individuálnej variability):
- 0–12 hodín: Organizmus primárne využíva glukózu a glykogén. Autofágia prebieha na bázovej úrovni.
- 12–16 hodín: V mnohých modeloch sa pozoruje zvýšená aktivácia signálnych dráh spojených s bunkovou recykláciou, najmä v pečeňovom tkanive.
- 16+ hodín: Výraznejší prechod na oxidáciu mastných kyselín, produkcia ketolátok. Tento metabolický stav koreluje s robustnejšou autofagickou aktivitou.
Presný čas závisí od metabolického stavu, posledného jedla, pohybovej aktivity a cirkadiánnych rytmov. Tieto čísla sú orientačné — nie predpis.
5. Čo s tým urobiť: tri prístupy podľa cieľa
Toto nie je protokol. Je to prehľad prístupov, ktoré výskum spája s rôznymi cieľmi — s upozornením, že každý individuálny kontext je iný.
Denná údržba — 16:8 Jedenie v 8-hodinovom okne, 16 hodín bez kalorického príjmu. Podľa Longo & Panda (2016, Cell Metabolism) tento rytmus koreluje so zlepšením metabolických markerov aj bez redukcie celkového kalorického príjmu. Mechanizmus: pravidelné fázy nízkej inzulínovej stimulácie umožňujú bazálnu autofágiu fungovať efektívnejšie.
Týždenný reset — 24-hodinový pôst Raz za 7–14 dní. Spája sa s hlbšou aktiváciou autofágie a stimuláciou kmeňových buniek po refeedingu. Vyžaduje viac prípravy — refeeding (prvé jedlo po pôste) je rovnako dôležitý ako samotný pôst: kvalitné aminokyseliny a esenciálne lipidy pre obnovu bunkových štruktúr.
Fyzická aktivita nalačno Pohyb pri nízkej dostupnosti glykogénu urýchľuje mitofágiu — elimináciu poškodených mitochondrií. Nie je to pre každého — a nie je to „lepší“ tréning. Je to špecifický stimul pre bunkové upratovanie.
Dôležité upozornenie: Pôst nie je vhodný pre každého. Tehotné ženy, osoby s poruchami príjmu potravy, diabetici a ľudia s určitými ochoreniami by mali akékoľvek zmeny konzultovať s lekárom.
Záver: bunka, ktorá nikdy neupratuje
Yoshinori Ohsumi nám dal biologický jazyk pre niečo, čo evolúcia vedela vždy: organizmus potrebuje rytmus. Nie nepretržitý prísun, ale osciláciu medzi sýtosťou a deficitom.
Moderná výživa tento rytmus výrazne skrátila — nie zrušila. Telo upratuje stále. Otázka je len, či mu dávame dostatok priestoru na to, aby upratovalo efektívne. Snack kultúra, jedenie každé tri hodiny, stravovanie do neskorých hodín (3-6 hodín pred spánkom) — každé z týchto rozhodnutí predlžuje čas, počas ktorého mTOR beží a autofágia čaká.
Výsledok nie je dramatický ani okamžitý. Je pomalý a kumulatívny: poškodené mitochondrie sa hromadia, proteínové agregáty sa nestihnú odstrániť, imunitné bunky starnú bez regenerácie.
Biologická prosperita často nezávisí od toho, čo do systému pridáte. Závisí od toho, čo mu v správnom čase dovolíte recyklovať.
Zoznam literatúry
- Ohsumi, Y. (2014) — Historical landmarks of autophagy research — Cell Research, 24(1): 9–23
- Mattson, M. P. et al. (2018) — Intermittent metabolic switching, neuroplasticity and brain health — Nature Reviews Neuroscience, 19(2): 63–80
- Longo, V. D. & Panda, S. (2016) — Fasting, circadian rhythms, and time-restricted feeding in healthy lifespan — Cell Metabolism, 23(6): 1048–1059
- Levine, B. & Kroemer, G. (2019) — Biological functions of autophagy genes: a disease perspective — Cell, 176(1–2): 11–42
- Saxton, R. A. & Sabatini, D. M. (2017) — mTOR signaling in growth, metabolism, and disease — Cell, 168(6): 960–976